El fin del cerrojo farmacéutico: la historia detrás de la resolución de patentes que dividió a los laboratorios durante décadas
En un gesto clave hacia la administración de Estados Unidos, la Argentina eliminó las trabas a la propiedad intelectual farmacéutica vigentes desde 2012; fue una histórica pelea entre las empresas nacionales y extranjeras
 8 minutos de lectura'
8 minutos de lectura'


Pocas cosas dividieron aguas en un negocio como la ley de patentes en el mundo de los laboratorios. Durante años, los “extranjeros” y los “nacionales” ni siquiera se sentaban en la misma mesa. Las cámaras sectoriales siempre fueron dos. Por un lado, Cilfa, que agrupa a los locales; por el otro, Caeme, que hace lo propio con las filiales de los internacionales. Cada una expresó muchas veces opiniones contrarias.
Esa disputa tenía una razón: las patentes de los medicamentos. Hoy, las restricciones que estaban vigentes para anotar un medicamento como propio fueron removidas por una resolución del Gobierno. Y entonces, todo podría cambiar en el lucrativo negocio.
A modo de resumen, los extranjeros querían que les respeten las patentes de sus innovaciones o invenciones, que en el mundo se protegen por 20 años; los otros, los nacionales, pretendían que se mantengan los procedimientos actuales, muy restrictivos a la hora de patentar un producto, y puedan seguir con los procesos de producción, muchas veces basados en la fórmula que la competencia presentaba en el regulador. Los primeros argumentan que la inversión en investigación no se paga en el país; los otros, que esa duplicación permite bajar los precios en el mostrador. Esos productos, en muchos casos, son los llamados genéricos.
El Gobierno, en el marco del acuerdo comercial con Estados Unidos, accedió a un viejo pedido que todos los años se repetía en uno de los reportes más importantes de la administración americana: avanzar en la protección de las patentes de productos medicinales y también en semillas. Por ahora, esto último, está pendiente. Pero para los laboratorios cambia el mercado.
Ahora bien, qué pasa con los consumidores. Pues ahí existe otra posición encontrada entre unos y otros. Desde Cilfa dicen que el precio subirá. “Los ahorros generados por el lanzamiento de medicamentos genéricos y biosimilares fueron estimados por la Fundación de Investigaciones Económicas Latinoamericanas (FIEL) en US$2214 millones anuales, a precios de septiembre de 2024. Si a esa suma se agregan los ahorros generados por nuevos lanzamientos o por moléculas no incluidas en el estudio de FIEL, el ahorro puede estimarse en el orden de los US$3321 millones para el año 2025. Esto implica no solo mayores ahorros para los gobiernos nacional, provinciales y municipales, así como para las obras sociales y las empresas de medicina prepaga, sino también una expansión de la cobertura a más pacientes, gracias a la posibilidad de los financiadores de tratar a más personas con menos recursos”, dijo la cámara mediante un comunicado.

El nuevo régimen funcionará como un mojón que empieza a generar efectos ahora, cuando formalmente se derogó una batería de regulaciones sancionadas en 2012. Entonces se acotó el sistema de protección de propiedad intelectual que establecía la ley de patentes, sancionada en los 90. Esas resoluciones fueron gestadas por Juan Manzur, entonces ministro de Salud, y Débora Giorgi, de Industria, y apoyadas con énfasis por los laboratorios de capitales nacionales.
Desde esta derogación de esas normas, que restringían la posibilidad de patentar una invención, ahora los laboratorios podrán traer sus productos y los demás no podrán copiar su fórmula y ofrecer uno similar. Pero nada es retroactivo y lo que ya está en el mercado no tendrá cambios. Es decir, los productos similares a los originales que se venden en las góndolas mantendrán su lugar.

La protección de la propiedad intelectual sobre un producto tiene una duración de 20 años. En ese tiempo no es posible que alguien reproduzca la fórmula y replique el medicamento. Según explican en Caeme, la cámara de los laboratorios extranjeros, en realidad, esas dos décadas de exclusividad son “engañosas”. Sucede que el procedimiento de inscripción de una invención empieza en un organismo técnico, el INPI, Instituto Nacional del Propiedad Intelectual. Esas inscripción es muy al inicio, incluso antes de que empiecen las pruebas de fase 1 (en aminales), 2 (en un grupo pequeño de humanos) y 3, ya masivamente. Ese proceso, dicen, puede durar varios años.
Después que efectivamente están esta pruebas, llega otra cuestión regulatoria: la inscripción en la Anmat, el organismo de contralor de medicamentos. Ese trámite, en el que se pide permiso para vender el producto en el país, dura alrededor de dos años. En conclusión, dicen en Caeme, la protección real desde que se empieza a vender, es de alrededor de 10 años.
En Cilfa no opinan lo mismo. Dicen que la industria farmacéutica hace abuso de las denominadas solicitudes de patentes de evergreening. Se trata de patentes que protegen innovaciones menores relativas a medicamentos ya conocidos (por caso, que una dosis mayor genera algún efecto en otra patología). Cuando eso sucede, los organismos extienden el uso de la patente. “No aportan efectos terapéuticos ni ningún otro valor, salvo preservar monopolios y obstaculizar durante años el lanzamiento de medicamentos competidores”, dice el comunicado de la cámara.
Uno de los casos más paradigmáticos de los últimos tiempos es la droga llamada semaglutida, utilizada para hacer el famoso medicamento para adelgazar cuyo nombre comercial es Ozempic. La firma que lo creó, el gigante danés Novo Nordisk, decidió venderlo en la Argentina pese a que no tenía una ley de patentes vigente y que podía ser copiado. Para hacerlo, presentó toda la fórmula y los requisitos en el Anmat, el organismo regulador argentino.
Poco tiempo después de que salió a la venta, Elea, el poderoso laboratorio de la familia Sigman-Gold, lanzó una copia llamada Dutide, a un precio, según Cilfa, 63,5% inferior. ¿Cómo lo hizo? Pues en la Argentina la fórmula que se presenta en la Anmat no está protegida y es de acceso al resto de los competidores. De esa manera es posible la réplica con el detalle exacto de los componentes.
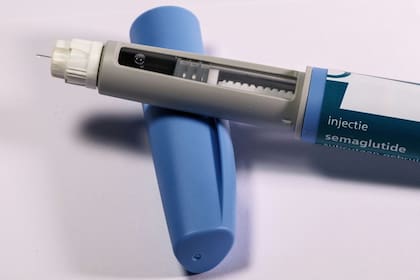
El ejemplo de esta droga es una muestra cabal del asunto. Para unos es la posibilidad concreta de llegar a más personas con la misma droga a un precio menor; para otros es casi un robo de un trabajo científico desarrollado por décadas.
“Durante más de una década, la normativa local hizo extremadamente difícil patentar medicamentos en el país ¿El resultado? Menos incentivos para invertir y menos innovación disponible -comunicó la Cámara de Comercio de los Estados Unidos en la Argentina (AmCham) mediante un posteo en X-. A partir de ahora, la Argentina avanza hacia un esquema más previsible y alineado con estándares internacionales en materia de evaluación de patentes. Mayor previsibilidad y reglas claras. Esto no es solo una norma técnica. Es una señal. La Argentina vuelve a generar condiciones para atraer inversión, desarrollar conocimiento y competir globalmente."
Justamente en este punto hay otra controversia. Los laboratorios extranjeros dicen que es necesario que también se avance en la protección de esta información llamada “datos de prueba” y por eso dicen que lo que sucedió en estas horas es sólo el inicio de un proceso para respetar la propiedad intelectual. Los locales opinan lo contrario.
Hay algo más: suscribir o no el tratado internacional. Falta la firma del acuerdo global. Se trata del Tratado de Cooperación en materia de Patentes (PCT), un sistema internacional gestionado por la World Intellectual Property Organization (WIPO) que permite tramitar la protección por patente en más de 150 países con una única “solicitud internacional”, algo así como una validación compartida.
Los voceros de los laboratorios internacionales argumentan que esta desprotección no solo afecta a los laboratorios, sino a muchos investigadores del Conicet o de institutos privados, por caso, que deciden volar a Brasil y anotar allí la innovación para tener el resguardo necesario. Ese proyecto para adherir al régimen internacional tienen que recorrer el camino parlamentario en el Congreso.
La AmCham, en su posteo, sostiene que una de las consecuencias de lo que sucedía antes es que los laboratorios no hacían investigaciones clínicas en el país. Fuentes del sector estiman la inversión en este área de los laboratorios internaciones en alrededor de US$700 millones y dicen que se podría triplicar. Cuentan que estos estudios generan no solo el beneficio de ese desembolso, sino que producen un ahorro en el sistema de salud, ya que los pacientes que están dentro del programa son solventados íntegramente por el laboratorio que realiza la prueba. Como beneficio adicional, explican, el país tiene acceso más rápido al medicamento, una vez aprobado.
“Confiamos en la idoneidad y la capacidad técnica del INPI para que continúe realizando el análisis de patentabilidad de manera rigurosa y sobre bases científicas, concediendo patentes a auténticas innovaciones farmacéuticas y rechazando las patentes de evergreening“, dijeron en Cilfa.
Así las cosas, formalmente se derogó la resolución conjunta 118/2012 (Industria), 546/2012 (Salud) y 107/2012 (INPI), llamada “Pautas para el Examen de Patentabilidad de las Solicitudes de Patentes sobre Invenciones Químico-Farmacéuticas”. El mercado hablará a mediano plazo. La Argentina pasó de un sistema que priorizaba el acceso rápido a genéricos mediante criterios de patentabilidad muy restrictivos y fomento a la copia, a un sistema que pone el foco en la protección del inventor para fomentar la innovación y la integración al comercio global.
 1
1Fecha de cobro de Anses: el cronograma de pagos para este martes 17 de marzo
 2
2“Hay mucha gente queriendo meterse”: subieron un 10% los precios en el triángulo de oro del mercado de campos
 3
3Importante acuerdo: llegaron desde China 45 vagones para la cosecha
 4
4El Gobierno defiende el modelo de cielos abiertos y busca consolidar la apertura del mercado




