¿ADN desgastado?: un experimento de 20 años reveló un límite inesperado de la clonación y abre nuevas preguntas
El ensayo, que sumó más de 30.000 intentos y alcanzó 58 generaciones, demostró que la línea clonal acumula mutaciones dañinas que la terminan volviéndola inviable
 5 minutos de lectura'
5 minutos de lectura'

Durante veinte años, un grupo de investigadores japoneses repitió una misma maniobra miles de veces: tomar una célula de un ratón, transferir su núcleo a un óvulo al que previamente se le había retirado el propio, y generar así un clon. Luego repetir ese proceso con ese clon, y con el clon siguiente, de manera ininterrumpida. El experimento, que sumó más de 30.000 intentos y alcanzó 58 generaciones, terminó revelando un límite hasta ahora desconocido para la clonación de mamíferos: incluso si los animales vivos parecen sanos, la línea clonal acumula mutaciones dañinas que terminan volviéndola inviable.
Los resultados, publicados en Nature Communications y difundidos por Nature, muestran que los ratones clonados podían alimentarse, vivir una vida normal e incluso reproducirse, pero al mismo tiempo cargaban mutaciones cada vez más agresivas. En los últimos estadios de la línea aparecieron cambios estructurales masivos en el ADN, como la pérdida completa de un cromosoma o grandes fragmentos de cromosomas duplicados, intercambiados o borrados. En la generación 58, ningún embrión logró desarrollarse. La línea colapsó.
“Este estudio es la primera demostración experimental de que, si la reproducción asexual continúa en mamíferos, las mutaciones se acumulan y finalmente llevan al cese del linaje”, explicó a Nature Atsuo Ogura, especialista en biología reproductiva del RIKEN BioResource Research Center. Para él, el hallazgo no solo explica por qué ningún mamífero se reproduce naturalmente por clonación, sino que tiene consecuencias directas para la agricultura y la conservación de especies.
Michael Lynch, biólogo evolutivo de la Universidad Estatal de Arizona, fue aún más explícito en su interpretación: “Esto probablemente se generaliza a cualquier tipo de clonación vertebrada, lo que tiene enormes implicancias para la agricultura. En cualquier programa de cría, si uno tuviera el genoma óptimo, la mejor manera de preservarlo sería clonarlo. Excepto por este problema de las mutaciones”.
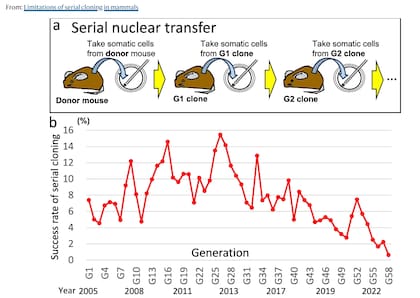
Los investigadores japoneses llevan décadas explorando los límites de la clonación. Teruhiko Wakayama y su equipo lograron clonar ratones incluso a partir de animales muertos durante años, tejidos congelados sin protección y células halladas en la orina. Pero este experimento apuntaba a una pregunta distinta: ¿se puede sostener indefinidamente un linaje de clones sin recurrir a la reproducción sexual? Durante un tiempo pareció que sí. Los primeros 25 ciclos no mostraron signos de deterioro, y los ratones nacían con tasas crecientes de éxito. Pero alrededor de la generación 27 comenzó la caída: la tasa de nacimiento descendió de manera sostenida y, hacia el final, los embriones dejaban de desarrollarse.
El grupo analizó entonces las posibles causas. Las marcas epigenéticas —las señales químicas que regulan la actividad de los genes— no parecían acumular errores con el paso de las generaciones. El problema estaba en otro lado: en la secuencia del ADN. Con cada clonación, el genoma sumaba alrededor de 70 mutaciones nuevas y al menos una mutación estructural grande. En los estadios finales aparecieron pérdidas de cromosomas, deleciones de cientos de miles de bases, inversiones de regiones completas y una translocación entre los cromosomas 7 y 9.
Esa acumulación acelerada coincide con un viejo concepto de la genética evolutiva, conocido como “el trinquete de Müller”, que predice que en líneas sin recombinación sexual las mutaciones perjudiciales se acumulan sin vuelta atrás hasta volverse letales. Después de veinte años de trabajo continuo, los investigadores creen haber demostrado por primera vez ese mecanismo en un mamífero.
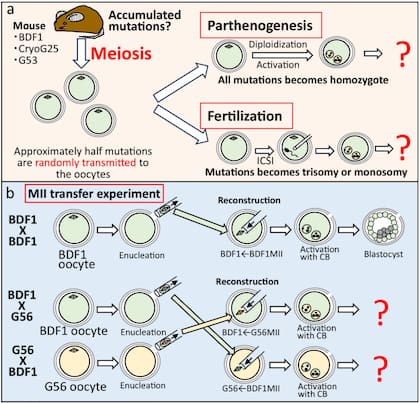
Aunque los ratones vivos parecían saludables, el estudio reveló otro dato crucial: la capacidad reproductiva también se degradaba. Las hembras clonadas de las generaciones tardías podían ser fecundadas, pero sus embriones degeneraban masivamente. Solo cuando esos óvulos se fertilizaban con esperma de ratones sanos —lo que reintroduce la recombinación sexual— algunos embriones lograban “normalizar” su desarrollo y llegar a término. La reproducción sexual funcionó como una suerte de reparación genética de emergencia.
Para la Argentina, el hallazgo toca un punto sensible. Desde hace dos décadas, el país se posicionó como uno de los centros mundiales de clonación animal aplicada a la producción: toros con genética sobresaliente, vacas superproductoras, caballos de polo y animales de elite que se replican para preservar una combinación genética considerada excepcional. A diferencia de países donde el uso comercial está más restringido, la clonación forma parte del ecosistema biotecnológico argentino y convive con mercados que demandan animales casi “idénticos” para competencias, reproducción o exportación de genética.
El nuevo estudio no cuestiona la clonación en sí: clonar un animal de alto valor sigue siendo viable, y el producto inmediato no exhibe inconvenientes visibles. Lo que sí pone en duda es una práctica que algunos criadores y laboratorios empezaron a explorar: reclonar clones, es decir, repetir el proceso sobre generaciones sucesivas como forma de mantener “pura” una línea o evitar la variabilidad que introduce la reproducción sexual.
Los investigadores japoneses señalan que eso es justamente lo que no funciona en mamíferos períodos sucesivos. Las mutaciones dañinas se acumulan, no se eliminan y terminan deteriorando la línea. Ogura lo plantea sin ambigüedades: “Si el objetivo es preservar animales superiores mediante clonación, es aconsejable almacenar una gran cantidad de células somáticas para usar como base y evitar la clonación seriada”.
En términos prácticos, esto implica que programas de clonación animal —ya sea en toros campeones, yeguas o caballos de polo de excelencia— deberían evitar generar clones de clones y, en cambio, volver siempre al material genético original o recurrir a la reproducción sexual para “limpiar” el genoma. La raíz misma de la evolución se impone: en mamíferos, la reproducción sexual es indispensable para sostener una línea en el tiempo.
Mientras sectores agroindustriales en la Argentina siguen viendo en la clonación una herramienta de valor estratégico, el experimento japonés ofrece un recordatorio biológico contundente: la perfección genética no puede conservarse por copiado indefinido.
 1
1Crecen los casos: otro virus transmitido por mosquitos desplaza al dengue este año
 2
2Fin de una batalla interminable: falleció el “hijo” que reclamó la herencia más polémica del país
 3
3La muerte de Noelia Castillo Ramos: por qué la justicia española avaló el pedido de eutanasia de la joven de 25 años
- 4
Qué pasó con Agostina Páez, la argentina acusada de racismo en Brasil






