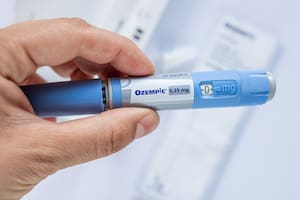
“Serias violaciones en el reporte de efectos adversos”: la dura advertencia de la FDA al laboratorio de Ozempic
La agencia señaló falencias en los procedimientos internos de Novo Nordisk, detectadas durante una inspección realizada en 2025
 5 minutos de lectura'
5 minutos de lectura'

La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) emitió una advertencia formal [Warning Letter] a Novo Nordisk por fallas graves en el reporte de efectos adversos asociados a dos de sus medicamentos más utilizados: Ozempic y Wegovy, ambos basados en semaglutida. La carta, fechada el 5 de marzo de 2026, se basa en una inspección realizada entre el 13 de enero y el 7 de febrero de 2025 en la sede que la compañía tiene en Plainsboro, Nueva Jersey.
Según el organismo, la empresa no cumplió con los plazos y procesos obligatorios para informar experiencias adversas graves e inesperadas, como exige la legislación estadounidense. Entre las principales observaciones, la FDA detectó que los procedimientos internos permitían rechazar reportes cuando los consumidores afirmaban que no existía relación aparente con el tratamiento, pese a que la normativa obliga a registrar todo evento grave ocurrido durante el uso del medicamento.

Uno de los episodios señalados corresponde a un paciente que sufrió un accidente cerebrovascular mientras recibía liraglutida, otro principio activo comercializado por la compañía. El informe no fue remitido a la FDA porque el propio consumidor entendía que el episodio no estaba vinculado al tratamiento. En otro caso, la agencia constató demoras importantes en la revisión médica de reportes de ideación suicida asociados al uso de semaglutida, utilizados en tratamientos con Ozempic y Wegovy, que debieron haberse informado dentro del plazo legal de 15 días.
La advertencia también indica deficiencias en la validación inicial de los reportes. La inspección verificó casos descartados por supuesta falta de identificadores del paciente, pese a que esa información sí figuraba en los documentos originales. Esto demoró o impidió la notificación de eventos graves, como la muerte de una persona que estaba en tratamiento con semaglutida.

Otro de los puntos cuestionados fue la ausencia de una investigación rápida en situaciones que exigían un seguimiento inmediato. En un caso, la muerte de un paciente tratado con semaglutida no fue investigada porque la notificación la había realizado un particular que no era profesional de la salud. En otro episodio, un médico informó que un paciente bajo tratamiento se suicidó, pero la compañía no efectuó intentos para obtener más información y el caso no fue reportado.
La carta nunca menciona los nombres comerciales Ozempic o Wegovy, pero sí identifica los principios activos involucrados. En varios pasajes señala que Novo Nordisk es responsable por el reporte de experiencias adversas asociadas a productos que contienen semaglutida, liraglutida, nedosiran sódico y estradiol, lo que incluye directamente a los medicamentos más difundidos de la compañía.

Para la FDA, estas fallas representan problemas sistémicos en la vigilancia, recepción y análisis de eventos adversos, además de deficiencias en la supervisión de los contratistas que gestionan los reportes de seguridad.
En la carta, la agencia exige a la empresa corregir todas las inconsistencias, actualizar sus procedimientos y asegurar el cumplimiento de los requisitos que rigen la notificación de efectos adversos. También solicita que Novo Nordisk presente, dentro de los próximos 15 días hábiles, un plan detallado con las medidas adoptadas para evitar nuevas infracciones.
La advertencia fue firmada por David C. Burrow, director de la Oficina de Investigaciones Científicas del CDER.
“No formula conclusiones”
En un comunicado enviado a medios de Estados Unidos, Novo Nordisk confirmó la recepción de la carta de advertencia de la FDA y señaló que la empresa estuvo “trabajando diligentemente para abordar las observaciones de la agencia desde la inspección realizada el año pasado”. Según la farmacéutica, el organismo regulador solicitó información adicional sobre las medidas implementadas para asegurar el cumplimiento de los requisitos que rigen la vigilancia poscomercialización.
La compañía destacó que la advertencia “no formula conclusiones sobre la calidad ni la seguridad de nuestros medicamentos”, en referencia a los productos que contienen semaglutida, como Ozempic y Wegovy. También aseguró que toma “muy en serio” las obligaciones de notificación de efectos adversos y que responderá a los pedidos del regulador “de manera expedita y holística”.
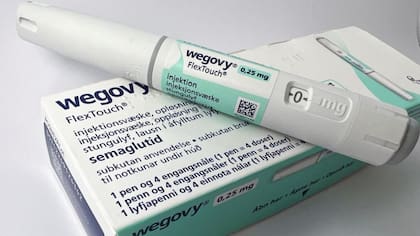
Novo Nordisk informó además que, tras la inspección realizada entre enero y febrero de 2025, implementó un plan de acciones correctivas y preventivas con el objetivo de ajustar sus procesos internos de reporte. La compañía indicó que desde entonces mantuvo un intercambio constante con la FDA y envió siete actualizaciones formales sobre el avance de esas medidas.
En su respuesta, la empresa sostuvo que las observaciones surgidas de la inspección no reflejan conclusiones sobre el perfil de seguridad de sus tratamientos, y subrayó que continuará colaborando con la autoridad sanitaria en cada una de las etapas del proceso regulatorio. Según la compañía, la advertencia busca principalmente verificar la consistencia de los sistemas de control y la aplicación uniforme de los procedimientos de farmacovigilancia.
Por último, Novo Nordisk afirmó que confía en poder resolver los puntos planteados por la FDA dentro de los plazos establecidos. “Estamos seguros de que podremos resolver los asuntos planteados en la Warning Letter a plena satisfacción de la agencia”, señaló la empresa en el comunicado difundido a la prensa.
 1
1Murió el niño de un año que estaba internado en Mendoza con lesiones cerebrales
 2
2Previo a la exhibición de Franco Colapinto, vecinos y comerciantes entre la expectativa y las quejas por la falta de información
 3
3Hay alerta amarilla por vientos, tormentas y nevadas para este sábado 25 de abril: las provincias afectadas
 4
4La psicología dice que venimos al mundo a desarmar lo que nos enseñaron y a aprender cosas nuevas